|
UWS Delfin Homberg e.V. |
|
Tauchphysik Gesetz von GayLussac |
|
Gay-Lussac - Druck und Temperatur Wenn wir eine Tauchflasche mit Pressluft füllen, können wir beobachten, dass sich die Flasche stark erwärmt. Wenn wir das Ventil öffnen und die Luft abströmen lassen, kühlt das Ventil so stark ab, dass sich eine Eisschicht bilden kann. Man kann sich daher denken, dass Druck und Temperatur in einem Verhältnis miteinander stehen müssen.
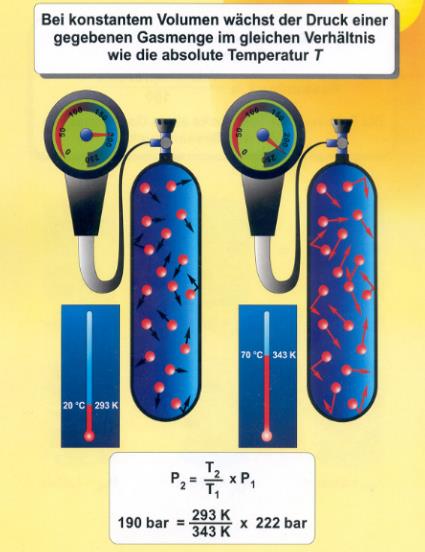
Bei gleichbleibendem Volumen wächst der Druck einer bestimmten Gasmenge im gleichen Verhältnis wie die absolute Temperatur: p/T = konstant
Damit kann man z.B. den Druckabfall berechnen, wenn man eine heiße Tauchflasche in kühles Wasser eintaucht:
Nehmen wir an, eine Flasche gefüllt mit 200 bar hat die Temperatur von 25° Celsius, was der Außentemperatur an einem schönen Sommertag entspricht. Das Wasser ist sehr kalt und hat eine Temperatur von nur 5°C. Mit dem Gesetz von Gay-Lussac kann man jetzt berechnen, wie hoch der Flaschendruck nach der Abkühlung auf 5°C ist: p1 = 200 bar
p1 p2 200 bar p2 200 bar * 278 K T1 T2 298 K 278 K 298 K p2 = 186,6 bar Durch die Abkühlung der Flasche reduziert sich also der Druck auf 186 bar. |

|
= |
|
= |
|
p2 = |
|
1.4 |